(2)甲基丙烯酸中含有的无氧官能团的称号是碳碳双键,含有的含氧官能团的结构式为
(3)0.3mol甲基丙烯酸与足量碳酸氢钠溶液反响,能生成标准状况下的CO26.73L.


(3)只要羧基能和碳酸氢钠反响,且甲基丙烯酸和生成二氧化碳的物质的量之比是1:1;
(5)甲基丙烯酸酸和甲醇产生酯化反响生成甲基丙烯酸甲酯,甲基丙烯酸甲酯产生加聚反响生成高分子化合物.
回答解:(1)按照结构简式知,分子式为C4H6O2,故答案为:C4H6O2;


(3)只要羧基能和碳酸氢钠反响,且甲基丙烯酸和生成二氧化碳的物质的量之比是1:1,所以0.3mol甲基丙烯酸和足量碳酸氢钠反响生成0.3mol二氧化碳,其体积=0.3mol×22.4L/mol=6.72L,
点评本题考察有机物结构和性质,为高频考点,清晰官能团及其性质联系是解本题要害,偏重考察烯烃和羧酸的性质,标题难度不大.
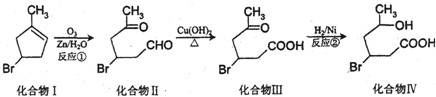
(1)化合物Ⅱ的分子式为C6H9O2Br;反响②的反响类型为加成反响;化合物IV中含有的官能团是羧基、羟基、溴原子.(写称号)
(3)化合物IV在浓硫酸催化下反响生成六元环状酯类化合物,写出该反响的化学方程式
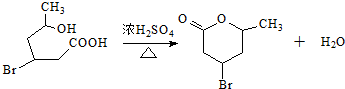
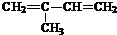
(2-甲基-1,3-丁二烯)产生相似①的反响,得到有机物VI和VII,结构简式分别是为
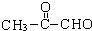
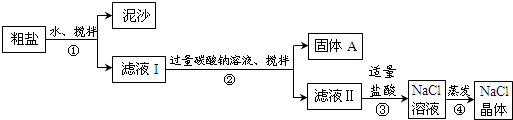
(1)为有用除掉粗盐中的Ca2+、Mg2+、SO42-等杂质,参加试剂的合理次序为BC.

②粗硅与氯气反响后得到的液态四氯化硅中常混有一些杂质,一定要进行别离提纯.其提纯办法为蒸馏.
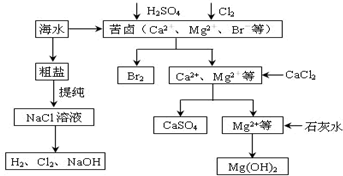
(4)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的次序制备?原因是否,假如先沉积Mg(OH)2,则沉积中会搀杂有CaSO4沉积,产品不纯.
(5)工业上选用电解MgCl2的办法制得金属镁,电解槽中阴极的电极反响式为Mg2++2e-=Mg,从MgCl2溶液得到MgCl2固体的办法是在氯化氢气流中加热蒸腾;有同学以为可加热Mg(OH)2得到MgO,再电解熔融MgO制金属镁,你赞同该同学的主意吗?为什么?不赞同,由于MgO熔点很高,熔融时消耗很多的能量而添加生产成本.
(2)假如平衡后坚持温度不变,将容器体积缩小为一半,新平衡时A的浓度是本来的2.2倍,则B是气态,C是气态.
(3)若B是气体,C不是,下列能阐明恒温恒容密闭容器中的反响已达到平衡①③④
①混合气体的密度不变②混合气体的压强不变③A的转化率不变④v正(A)=v逆(B)
(1)如图所示,设备气密性杰出,且1000mL量筒中已充满了水,则开端试验时,首要要用导线把a、b两电极连接起来.
(3)当量筒中收集到672mL气体时(已折算到标准状况下),经过导线mol.








